| [2013-003354-24] Influence de l’administration de l’hormone de croissance exogène sur les concentrations circulantes de a-klotho chez les sujets atteints d’insuffisance rénale chronique et en bonne santé : une étude pilote prospective monocentrique ouverte cas-témoins.
Aaltje Y. Adema, Camiel L. M. de Roij van Zuijdewijn, Joost G. Hoenderop, Martin H. de Borst, Piet M. Ter Wee, et al. Source : PLOS ONE | https://doi.org/10.1186/s12882-018-1114-z Télécharger “Table 2013-003354-24-ckd” 2013-003354-24-ckd.zip – Téléchargé 3 fois – 1,10 Mo Droit d’auteur : Utilisation des données du rapport sans restriction pourvu que l’auteur original et la source soient cités (données brutes libres de droits). |
| Sommaire |
| Méthodes |
| Objectif :
L’objectif de l’étude est d’évaluer l’effet de l’administration de l’hormone de croissance exogène (GH) sur les concentrations d’a-Klotho dans une cohorte clinique de patients atteints d’insuffisance rénale chronique légère (IRC) et de sujets sains. Évaluation : Une étude pilote cas-témoins ouverte prospective, monocentrique a été réalisée impliquant 8 patients atteints d’IRC et 8 témoins sains appariés pour l’âge et le sexe. Au total, 18 sujets (12 hommes et 6 femmes) avec et sans IRC de stade 3 selon la Chronic Kidney Disease Epidemiology Collaboration (CKD-EPI) ont été inclus pendant la période de janvier 2015 à mars 2016 en provenance de la clinique ambulatoire de néphrologie du centre médical VU, Amsterdam, Pays-Bas. Tous les sujets inclus ont reçu des injections sous-cutanées de GH pendant 7 jours consécutifs. Le critère d’évaluation principal est le changement des concentrations d’a-Klotho après 7 jours d’administration de GH. Le critère d’évaluation secondaire est la différence potentielle de variation de la concentration d’a-Klotho entre les patients atteints d’IRC et les sujets sains. Principes d’étude : Les variables qualitatives sont décrites avec des fréquences et des pourcentages de niveau (Pourcentages en colonne). Les variables quantitatives sont décrites avec des moyennes et écarts types, quartiles, minimum/maximum, intervalles de confiance à 95%. Les conditions de validité des tests paramétriques n’étant pas respectées : L’association entre un paramètre quantitatif et l’item « Groupe (GROUP) » a été évaluée avec le test de Mann-Whitney (MW). L’association entre un paramètre qualitatif et l’item « Groupe (GROUP) » a été évaluée avec le test exact de Fisher (Fs). Les analyses ont été réalisées à l’aide de régressions logistiques et linéaires mixtes. |
| Attention, au moins une sélection d’observation(s) a été réalisée sur la base de données initiale. |
| Codages et variables générées suite au gel de la base de données | |
|---|---|
| Variable(s) d’origine | Variable créée |
| Date de naissance (DATE_OF_BIRTH) | |
| Date de visite 1 (VISIT_DATE_1) | Age (AGE) issue d’une affectation (avec DATE_OF_BIRTH VISIT_DATE_1) |
| A-Klotho v2 (pg/mL) (AKLOTHO_2) | |
| A-Klotho v3 (pg/mL) (AKLOTHO_3) | A-Klotho (pg/mL) (AKLOTHO) issue d’un listage (de AKLOTHO_2 AKLOTHO_3) |
| Poids v1 (kg) (WEIGHT_1) | |
| Taille v1 (cm) (HEIGHT_1) | BMI (kg/m2) (BMI) issue d’une affectation (avec HEIGHT_1 WEIGHT_1) |
| CFGF23 v2 (RU/mL) (CFGF23_2) | |
| CFGF23 v3 (RU/mL) (CFGF23_3) | CFGF23 (RU/mL) (CFGF23) issue d’un listage (de CFGF23_2 CFGF23_3) |
| Group (GROUP) :
– 1 : CKD stage III – 2 : Healthy controls | Groupe (GROUP2) issue d’une affectation (avec GROUP) :
– 1 : IRC stade III – 2 : Groupe Contrôle |
| IGF-1 v2 (nmol/L) (IGF1_2) | |
| IGF-1 v3 (nmol/L) (IGF1_3) | IGF-1 (nmol/L) (IGF1) issue d’un listage (de IGF1_2 IGF1_3) |
| Group (GROUP) :
– 1 : CKD stage III – 2 : Healthy controls | |
| REPETITIONS | Visite selon Groupe (ORD_GROUP2_COD_VISIT) issue d’une ordinalisation :
– 1 : IRC stade III, Baseline – 2 : IRC stade III, Après 1 semaine de traitement GH – 3 : Groupe Contrôle, Baseline – 4 : Groupe Contrôle, Après 1 semaine de traitement GH |
| PTH v2 (pmol/L) (PTH_2) | |
| PTH v3 (pmol/L) (PTH_3) | PTH (pmol/L) (PTH) issue d’un listage (de PTH_2 PTH_3) |
| Phosphate sérique v2 (mmol/L) (SERUM_PHOSPHATE_2) | |
| Phosphate sérique v3 (mmol/L) (SERUM_PHOSPHATE_3) | Phosphate sérique (mmol/L) (SERUM_PHOSPHATE) issue d’un listage (de SERUM_PHOSPHATE_2 SERUM_PHOSPHATE_3) |
| Sex (SEX) :
– 1 : Male – 2 : Female | Sexe (SEX2) issue d’une affectation (avec SEX) :
– 1 : Masculin – 2 : Féminin |
| Smoking (SMOKING) :
– 0 : No – 1 : Yes | Fumeur (SMOKING2) issue d’une affectation (avec SMOKING) :
– 0 : Non – 1 : Oui |
| TMP/GFR v2 (mmol/L) (TMP_GFR_2) | |
| TMP/GFR v3 (mmol/L) (TMP_GFR_3) | TMP/GFR (mmol/L) (TMP_GFR) issue d’un listage (de TMP_GFR_2 TMP_GFR_3) |
| Excrétion urinaire de phosphate v2 (mmol/L) (URINARY_PHOSPHATE_2) | |
| Excrétion urinaire de phosphate v3 (mmol/L) (URINARY_PHOSPHATE_3) | Excrétion urinaire de phosphate (mmol/L) (URINARY_PHOSPHATE) issue d’un listage (de URINARY_PHOSPHATE_2 URINARY_PHOSPHATE_3) |
| REPETITIONS | Visite (VISIT) issue d’un conditionnement (sur REPETITIONS) :
– Après 1 semaine de traitement GH – Baseline |
| Tableau 1 : Codages |
| 1. Profil d’étude |
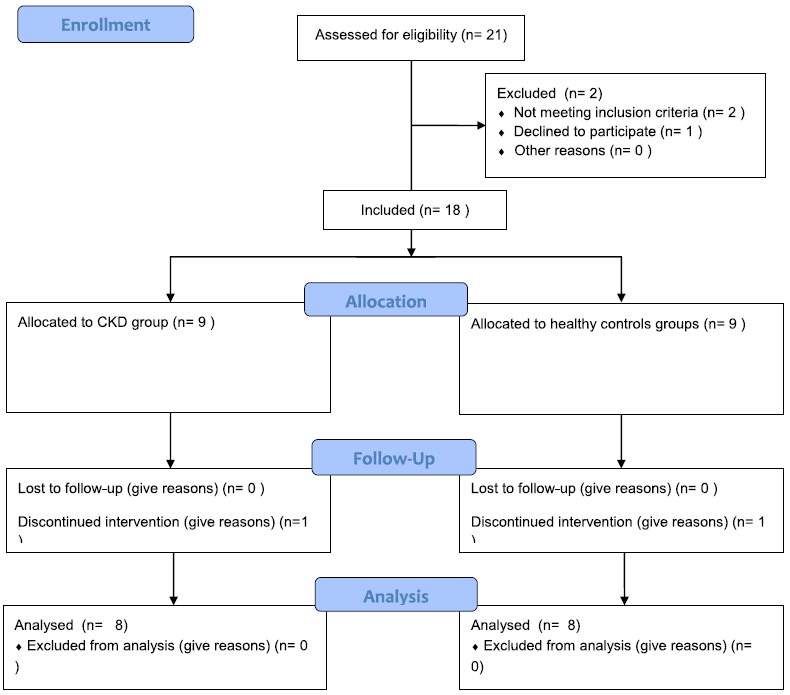
| 1.1. Flowchart |
| [Haut de page] |
| Flowchart |
| Les données de 16 sujets ont été analysées : 8 patients dans le groupe IRC et 8 dans le groupe témoin sain. |
| 2. Résultats |
| 2.1. Caractéristiques de base des participants |
| [Haut de page] |
| Les caractéristiques de base sont comparables entre les groupes, à l’exception de l’eGFR par définition des groupes. |
| Population | Groupe (GROUP2) | |||||||
|---|---|---|---|---|---|---|---|---|
| _ | IRC stade III | Groupe Contrôle | ||||||
| N=16 | N=8 | N=8 | ||||||
| Moy±SD
Méd(Q1Q3) Min-Max IC95% ou | Moy±SD
Méd(Q1Q3) Min-Max IC95% ou | Moy±SD
Méd(Q1Q3) Min-Max IC95% ou | Statistique | |||||
| Variable | n | %col | n | %col | n | %col | p | |
| Age (AGE) | Moyenne ±SD | 46 | ±11,66 | 47,13 | ±12,87 | 44,88 | ±11,09 | MW p = 0,4306 |
| Médiane (Q1-Q3) | 51,5 | (35,5-55,5) | 52,5 | (36,5-57,5) | 51,5 | (35-52,5) | ||
| Min-Max | 25 | 59 | 25 | 59 | 26 | 55 | ||
| IC à 95% | 39,79 | 52,21 | 36,37 | 57,88 | 35,6 | 54,15 | ||
| Sexe (SEX2) | Masculin | 10 | 62,5 | 5 | 62,5 | 5 | 62,5 | Fs p = 1,0000 |
| Féminin | 6 | 37,5 | 3 | 37,5 | 3 | 37,5 | ||
| Total | 16 | 100 | 8 | 50 | 8 | 50 | ||
| BMI (kg/m2) (BMI) | Moyenne ±SD | 24,5 | ±2,85 | 23,44 | ±2,78 | 25,71 | ±2,59 | MW p = 0,1832 |
| Médiane (Q1-Q3) | 24,56 | (21,56-27,64) | 22,12 | (21,48-25,81) | 26,09 | (23,76-27,79) | ||
| Min-Max | 20,69 | 28,38 | 20,69 | 28,02 | 21,16 | 28,38 | ||
| IC à 95% | 22,92 | 26,08 | 21,11 | 25,77 | 23,32 | 28,1 | ||
| Fumeur (SMOKING2) | Oui | 1 | 6,3 | 1 | 12,5 | 0 | 0 | Fs p = 1,0000 |
| Non | 15 | 93,8 | 7 | 87,5 | 8 | 100 | ||
| Total | 16 | 100 | 8 | 50 | 8 | 50 | ||
| SBP v2 (mmHg) (SBP_2) | Moyenne ±SD | 133,47 | ±10,85 | 133,94 | ±12,53 | 133 | ±9,74 | MW p = 0,7132 |
| Médiane (Q1-Q3) | 134,25 | (129,5-138) | 135,5 | (129,5-139,75) | 133 | (129-136,75) | ||
| Min-Max | 109 | 153 | 109 | 153 | 116 | 150,5 | ||
| IC à 95% | 127,69 | 139,25 | 123,46 | 144,41 | 124,86 | 141,14 | ||
| DBP v2 (mmHg) (DBP_2) | Moyenne ±SD | 80,13 | ±8,83 | 82,38 | ±10,69 | 77,88 | ±6,42 | MW p = 0,2691 |
| Médiane (Q1-Q3) | 79,75 | (74,25-85,75) | 82,25 | (77-89) | 78,5 | (73,5-83) | ||
| Min-Max | 63,5 | 99 | 63,5 | 99 | 67 | 86 | ||
| IC à 95% | 75,42 | 84,83 | 73,44 | 91,31 | 72,5 | 83,25 | ||
| EGFR v2 (ml/min/1.73 m2) (EGFR_2) | Moyenne ±SD | 62,83 | ±19,65 | 52 | ±14,06 | 84,5 | ±3,87 | MW p = 0,0085 |
| Médiane (Q1-Q3) | 59 | (51,5-82) | 54,5 | (43,5-59) | 85,5 | (82-87) | ||
| Min-Max | 28 | 88 | 28 | 74 | 79 | 88 | ||
| IC à 95% | 50,35 | 75,32 | 40,24 | 63,76 | 78,34 | 90,66 | ||
| IGF-1 v2 (nmol/L) (IGF1_2) | Moyenne ±SD | 26,75 | ±5,04 | 26,25 | ±2,76 | 27,25 | ±6,8 | MW p = 0,9150 |
| Médiane (Q1-Q3) | 27 | (24-27,5) | 26 | (24-28) | 27 | (24,5-27,5) | ||
| Min-Max | 18 | 42 | 23 | 31 | 18 | 42 | ||
| IC à 95% | 24,06 | 29,44 | 23,94 | 28,56 | 21,57 | 32,93 | ||
| Phosphate sérique v2 (mmol/L) (SERUM_PHOSPHATE_2) | Moyenne ±SD | 0,95 | ±0,16 | 0,89 | ±0,16 | 1,01 | ±0,16 | MW p = 0,1264 |
| Médiane (Q1-Q3) | 0,93 | (0,87-1,05) | 0,87 | (0,83-1) | 0,95 | (0,91-1,05) | ||
| Min-Max | 0,62 | 1,37 | 0,62 | 1,13 | 0,89 | 1,37 | ||
| IC à 95% | 0,86 | 1,04 | 0,76 | 1,02 | 0,87 | 1,14 | ||
| PTH v2 (pmol/L) (PTH_2) | Moyenne ±SD | 6,01 | ±2,67 | 7,34 | ±3,12 | 4,69 | ±1,25 | MW p = 0,0738 |
| Médiane (Q1-Q3) | 5,4 | (4,45-6,65) | 6,65 | (5,05-9,85) | 4,8 | (4,45-5,4) | ||
| Min-Max | 2 | 12,1 | 3,5 | 12,1 | 2 | 6,2 | ||
| IC à 95% | 4,59 | 7,44 | 4,73 | 9,95 | 3,64 | 5,73 | ||
| CFGF23 v2 (RU/mL) (CFGF23_2) | Moyenne ±SD | 98,75 | ±26,67 | 101,25 | ±26,65 | 96,25 | ±28,28 | MW p = 0,5635 |
| Médiane (Q1-Q3) | 96,5 | (80,5-116) | 99,5 | (83,5-126,5) | 92 | (80,5-103,5) | ||
| Min-Max | 59 | 157 | 59 | 132 | 61 | 157 | ||
| IC à 95% | 84,54 | 112,96 | 78,97 | 123,53 | 72,61 | 119,89 | ||
| Albumine v2 (g/L) (ALBUMIN_2) | Moyenne ±SD | 38,13 | ±2,09 | 38,25 | ±2,05 | 38 | ±2,27 | MW p = 0,9573 |
| Médiane (Q1-Q3) | 38,5 | (37-40) | 38 | (37-40) | 39 | (36,5-39,5) | ||
| Min-Max | 34 | 41 | 35 | 41 | 34 | 40 | ||
| IC à 95% | 37,01 | 39,24 | 36,53 | 39,97 | 36,1 | 39,9 | ||
| A-Klotho v2 (pg/mL) (AKLOTHO_2) | Moyenne ±SD | 587,56 | ±255,44 | 529 | ±131,96 | 646,13 | ±338,47 | MW p = 0,5992 |
| Médiane (Q1-Q3) | 553,5 | (406-657) | 553,5 | (393,5-657) | 546,5 | (433,5-689) | ||
| Min-Max | 358 | 1427 | 358 | 666 | 404 | 1427 | ||
| IC à 95% | 451,45 | 723,68 | 418,68 | 639,32 | 363,15 | 929,1 | ||
| Fs : Fisher, MW : Mann-Whitney | ||||||||
| Tableau 2 : Résultats – Caractéristiques de base des participants – Tri croisé |
| # BMI (kg/m2) (BMI) : 1 donnée non disponible, 1 individu dont l’item « Groupe (GROUP2) » est renseigné « Groupe Contrôle » |
| # EGFR v2 (ml/min/1.73 m2) (EGFR_2) : 4 données non disponibles, 4 individus dont l’item « Groupe (GROUP2) » est renseigné « Groupe Contrôle » |
| 2.2. Résultats liés au temps entre les groupes |
| [Haut de page] |
| Après 7 jours de traitement de supplémentation en GH (GHST), les concentrations moyennes d’IGF-1 sont significativement plus élevées.
Ainsi, elles passent de 26,3 ±2,8 nmol/L à 59,8 ±20,5 nmol/L (OR 1,265, IC à 95% 1,040 à 1,539) dans le groupe IRC et de 27,3 ±6,8 nmol/L à 63,6 ±15,6 nmol/L (OR 1,242, IC à 95% 1,222 à 1,262) pour les témoins sains. |
| Visite selon Groupe | |||||
|---|---|---|---|---|---|
| IRC stade III, Baseline | IRC stade III, Après 1 semaine de traitement GH | Groupe Contrôle, Baseline | Groupe Contrôle, Après 1 semaine de traitement GH | ||
| N=8 | N=8 | N=8 | N=8 | ||
| Variable | Moy±SD
Méd(Q1Q3) Min-Max IC95% | Moy±SD
Méd(Q1Q3) Min-Max IC95% | Moy±SD
Méd(Q1Q3) Min-Max IC95% | Moy±SD
Méd(Q1Q3) Min-Max IC95% | |
| IGF-1 (nmol/L) (IGF1) | Moyenne ±SD | 26,25±2,76 | 59,75±20,53 | 27,25±6,8 | 63,63±15,58 |
| Médiane (Q1-Q3) | 26(24-28) | 57(49,5-76,5) | 27(24,5-27,5) | 65(50,5-72,5) | |
| Min-Max | 23-31 | 24-88 | 18-42 | 43-90 | |
| IC à 95% | 23,94-28,56 | 42,59-76,91 | 21,57-32,93 | 50,6-76,65 | |
| Phosphate sérique (mmol/L) (SERUM_PHOSPHATE) | Moyenne ±SD | 0,89±0,16 | 0,87±0,19 | 1,01±0,16 | 1,11±0,26 |
| Médiane (Q1-Q3) | 0,87(0,83-1) | 0,88(0,7-1,01) | 0,95(0,91-1,05) | 1,08(0,91-1,22) | |
| Min-Max | 0,62-1,13 | 0,65-1,16 | 0,89-1,37 | 0,81-1,63 | |
| IC à 95% | 0,76-1,02 | 0,71-1,03 | 0,87-1,14 | 0,89-1,32 | |
| Excrétion urinaire de phosphate (mmol/L) (URINARY_PHOSPHATE) | Moyenne ±SD | 17,41±9,31 | 14,43±5,75 | 23,09±10,9 | 35,96±21,96 |
| Médiane (Q1-Q3) | 14,8(12,85-17,3) | 14,55(9,4-19,65) | 20,35(14,25-31,7) | 27,3(19,45-60,3) | |
| Min-Max | 9,9-39,5 | 6,2-22 | 10,8-41,3 | 10,1-63,5 | |
| IC à 95% | 9,63-25,2 | 9,62-19,23 | 13,97-32,2 | 17,6-54,32 | |
| TMP/GFR (mmol/L) (TMP_GFR) | Moyenne ±SD | 0,62±0,14 | 0,63±0,17 | 0,91±0,23 | 1,02±0,41 |
| Médiane (Q1-Q3) | 0,61(0,54-0,68) | 0,61(0,51-0,76) | 0,82(0,77-0,97) | 0,93(0,73-1,15) | |
| Min-Max | 0,39-0,88 | 0,38-0,92 | 0,74-1,44 | 0,65-1,93 | |
| IC à 95% | 0,5-0,74 | 0,49-0,77 | 0,71-1,11 | 0,68-1,37 | |
| PTH (pmol/L) (PTH) | Moyenne ±SD | 7,34±3,12 | 6,4±2,31 | 4,69±1,25 | 5,24±1,18 |
| Médiane (Q1-Q3) | 6,65(5,05-9,85) | 6,5(4,75-7,7) | 4,8(4,45-5,4) | 5,5(4,3-6) | |
| Min-Max | 3,5-12,1 | 3-10,3 | 2-6,2 | 3,5-6,8 | |
| IC à 95% | 4,73-9,95 | 4,47-8,33 | 3,64-5,73 | 4,25-6,23 | |
| CFGF23 (RU/mL) (CFGF23) | Moyenne ±SD | 101,25±26,65 | 129,13±16,37 | 96,25±28,28 | 120,63±23,29 |
| Médiane (Q1-Q3) | 99,5(83,5-126,5) | 132,5(116-138,5) | 92(80,5-103,5) | 114(102,5-134,5) | |
| Min-Max | 59-132 | 105-154 | 61-157 | 98-165 | |
| IC à 95% | 78,97-123,53 | 115,44-142,81 | 72,61-119,89 | 101,15-140,1 | |
| A-Klotho (pg/mL) (AKLOTHO) | Moyenne ±SD | 529±131,96 | 625,38±325,07 | 646,13±338,47 | 711,88±256,32 |
| Médiane (Q1-Q3) | 553,5(393,5-657) | 590,5(366-718) | 546,5(433,5-689) | 654(538,5-748) | |
| Min-Max | 358-666 | 331-1323 | 404-1427 | 511-1303 | |
| IC à 95% | 418,68-639,32 | 353,61-897,14 | 363,15-929,1 | 497,59-926,16 | |
| Tableau 3 : Résultats – Résultats liés au temps entre les groupes – Tri croisé |
| Visite selon Groupe (ORD_GROUP2_COD_VISIT) | |||||
|---|---|---|---|---|---|
| IRC stade III, Après 1 semaine de traitement GH | Groupe Contrôle, Baseline | Groupe Contrôle, Après 1 semaine de traitement GH | |||
| N=8 | N=8 | N=8 | |||
| Variable | OR*[IC95%] | OR*[IC95%] | OR*[IC95%] | p | |
| IGF-1 (nmol/L) (IGF1) | Ref – IRC stade III, Baseline
1,265[1,040 ; 1,539] | Ref – IRC stade III, Baseline
1,033[0,861 ; 1,240] | Ref – IRC stade III, Baseline
1,283[1,052 ; 1,565] | Wd p = 0,0410 | |
| Phosphate sérique (mmol/L) (SERUM_PHOSPHATE) | Ref – IRC stade III, Baseline
0,449[<0,001 ; 275,3] | Ref – IRC stade III, Baseline
62,99[0,112 ; >999] | Ref – IRC stade III, Baseline
578,9[0,769 ; >999] | Wd p = 0,1670 | |
| Excrétion urinaire de phosphate (mmol/L) (URINARY_PHOSPHATE) | Ref – IRC stade III, Baseline
0,938[0,805 ; 1,093] | Ref – IRC stade III, Baseline
1,052[0,949 ; 1,166] | Ref – IRC stade III, Baseline
1,103[0,994 ; 1,225] | Wd p = 0,1037 | |
| TMP/GFR (mmol/L) (TMP_GFR) | Ref – IRC stade III, Baseline
2,047[0,002 ; >999] | Ref – IRC stade III, Baseline
>999[6,820 ; >999] | Ref – IRC stade III, Baseline
>999[18,53 ; >999] | Wd p = 0,0559 | |
| PTH (pmol/L) (PTH) | Ref – IRC stade III, Baseline
0,846[0,552 ; 1,298] | Ref – IRC stade III, Baseline
0,471[0,234 ; 0,945] | Ref – IRC stade III, Baseline
0,600[0,331 ; 1,088] | Wd p = 0,1638 | |
| CFGF23 (RU/mL) (CFGF23) | Ref – IRC stade III, Baseline
1,055[1,003 ; 1,110] | Ref – IRC stade III, Baseline
0,990[0,948 ; 1,034] | Ref – IRC stade III, Baseline
1,037[0,990 ; 1,087] | Wd p = 0,0859 | |
| A-Klotho (pg/mL) (AKLOTHO) | Ref – IRC stade III, Baseline
1,002[0,997 ; 1,008] | Ref – IRC stade III, Baseline
1,003[0,997 ; 1,008] | Ref – IRC stade III, Baseline
1,003[0,998 ; 1,009] | Wd p = 0,6362 | |
| Wd : Wald *OR : Odds Ratio | |||||
| Tableau 4 : Résultats – Résultats liés au temps entre les groupes – Forces d’association |
| 2.3. Analyse des concentrations d’AKlotho avec modèle mixte multivarié |
| [Haut de page] |
| Les concentrations d’a-Klotho ne sont ni significativement différentes entre les patients IRC et les témoins sains (p = 0,4089), ni significativement différentes après 7 jours de GHST (p = 0,1015). |
| A-Klotho (pg mL) (AKLOTHO) | |||
|---|---|---|---|
| N=32 | n=32 | ||
| Variable | MD*[IC95%] | Wd p | |
| Groupe (GROUP2) | IRC stade III | 0 | 0,4089 |
| Groupe Contrôle | 86,500[-181,8 ; 354,83] | ||
| Visite (VISIT) | Après 1 semaine de traitement GH | 0 | 0,1015 |
| Baseline | -96,38[-252,2 ; 59,487] | ||
| Wd : Wald *MD : Mean Difference | |||
| Tableau 5 : Résultats – Analyse des concentrations d’AKlotho avec modèle mixte multivarié – Forces d’association en analyse multivariée |
| Tables et figures |
| Tableau 1 : Codages |
| Tableau 2 : Résultats – Caractéristiques de base des participants – Tri croisé |
| Tableau 3 : Résultats – Résultats liés au temps entre les groupes – Tri croisé |
| Tableau 4 : Résultats – Résultats liés au temps entre les groupes – Forces d’association |
| Tableau 5 : Résultats – Analyse des concentrations d’AKlotho avec modèle mixte multivarié – Forces d’association en analyse multivariée |
| Figure 1 : Profil d’étude – Flowchart – Flowchart |
| Date de réalisation : 3 juin 2021 |
| Réalisateur : RUS |
| Logiciel version 0.1 |