| [2013-001665-16] Sufentanil intranasal versus morphine intraveineuse pour la douleur traumatique aiguë sévère : Une étude de non-infériorité randomisée en double aveugle.
Blancher M, Maignan M, Clapé C, Quesada J-L, Collomb-Muret R, Albasini F, et al. Source : PLOS ONE | https://doi.org/10.1371/journal.pmed.1002849 Télécharger “Table 2013-001665-16-algofine” 2013-001665-16-algofine.zip – Téléchargé 7 fois – 1,59 Mo Droit d’auteur : Utilisation des données du rapport sans restriction pourvu que l’auteur original et la source soient cités (données brutes libres de droits). |
| Sommaire |
| Méthodes |
| Objectif :
L’objectif de l’étude est de déterminer si le sufentanil intranasal (INS) pour les patients se présentant à un service d’urgence avec une douleur traumatique aiguë sévère entraîne une réduction de l’intensité de la douleur non-inférieure à la morphine intraveineuse (IVM). Évaluation : Un essai de non-infériorité prospectif, randomisé et multicentrique a été mené dans les services d’urgence de 6 hôpitaux à travers la France. Au total, 194 patients souffrant de douleurs traumatiques aiguës ont été évalués pour l’éligibilité entre le 4 novembre 2013 et le 10 avril 2015 : 157 ont été inclus dans la cohorte des urgences et randomisés, 155 ont commencé le traitement et 136 ont respecté les administrations du protocole (69 groupe IVM, 67 groupe INS). Les patients ont été randomisés en 1:1 pour recevoir une titration INS (0,3 µg/kg et des doses supplémentaires de 0,15 µg/kg à 10 minutes et 20 minutes si l’échelle numérique d’évaluation de la douleur [NRS] était supérieure à 3) et un placebo par voie intraveineuse, ou à l’IVM (0,1 mg/ kg et doses supplémentaires de 0,05 mg/kg à 10 minutes et 20 minutes si l’évaluation NRS était supérieure 3) et placebo intranasal. Le critère d’évaluation principal est l’efficacité de l’analgésie définie comme une diminution de la douleur sur la NRS entre la première administration et 30 minutes plus tard dans la population per protocole. La marge de non-infériorité prédéfinie est de -1,3 sur la NRS. Les critères d’évaluation secondaires incluent l’efficacité de l’analgésie à 10 et 20 minutes définie par une diminution du NRS, et l’incidence de tout événement indésirable grave et non grave jusqu’à 4 heures après la première administration. Principes de l’étude : Les variables qualitatives sont décrites avec des fréquences et des pourcentages de niveau (pourcentages en colonne). Les variables quantitatives sont décrites avec des moyennes et des écarts types, quartiles, minimum/maximum, intervalles de confiance à 95%. L’association entre un paramètre quantitatif et l’item « Groupe de randomisation (GROUP2) » a été évaluée avec le test de Student(Sd). L’association entre un paramètre qualitatif et l’item « Groupe de randomisation (GROUP2) » a été évaluée avec le test du Khi2(K2). Les analyses ont été effectuées à l’aide de régressions linéaires appariées. |
| Attention, au moins une sélection d’observation(s) a été réalisée sur la base de données initiale. |
| Codages et variables générées suite au gel de la base de données | |
|---|---|
| Variable(s) d’origine | Variable créée |
| Allergy is observed (ALLERGY) :
– 0 : No – 1 : Yes | Une allergie est observée (ALLERGY2) issue d’une affectation (avec ALLERGY) :
– 0 : Non – 1 : Oui |
| An anaphylactic_shock is observed (ANAPHYLACTIC_SHOCK) :
– 0 : No – 1 : Yes | Un choc anaphylactique est observé (ANAPHYLACTIC_SHOCK2) issue d’une affectation (avec ANAPHYLACTIC_SHOCK) :
– 0 : Non – 1 : Oui |
| Bad_taste is declared (BAD_TASTE) :
– 0 : No – 1 : Yes | Le mauvais goût est déclaré (BAD_TASTE2) issue d’une affectation (avec BAD_TASTE) :
– 0 : Non – 1 : Oui |
| A heart rate bpm <45/min is observed (BRADYCARDIA) :
– 0 : No – 1 : Yes | Une fréquence cardiaque bpm <45/min est observée (BRADYCARDIA2) issue d’une affectation (avec BRADYCARDIA) :
– 0 : Non – 1 : Oui |
| A Respiratory rate <10/minute is observed (BRADYPNEA) :
– 0 : No – 1 : Yes | Une fréquence respiratoire <10/minute est observée (BRADYPNEA2) issue d’une affectation (avec BRADYPNEA) :
– 0 : Non – 1 : Oui |
| Centre of inclusion (CENTRE) | Centre d’inclusion (CENTRE2) issue d’un conditionnement (sur CENTRE) :
– Albertville – Annecy – Chambery – Grenoble (Site nord) – Grenoble (Site sud) – Saint-Jean-de-Maurienne – Voiron |
| A Ramsay score >2 is observed (COMA) :
– 0 : No – 1 : Yes | Un score de Ramsay > 2 est observé (COMA2) issue d’une affectation (avec COMA) :
– 0 : Non – 1 : Oui |
| Dizziness is observed or declared (DIZZINESS) :
– 0 : No – 1 : Yes | Des vertiges sont observés ou déclarés (DIZZINESS2) issue d’une affectation (avec DIZZINESS) :
– 0 : Non – 1 : Oui |
| Epistaxis is observed or declared (EPISTAXIS) :
– 0 : No – 1 : Yes | L’épistaxis est observée ou déclarée (EPISTAXIS2) issue d’une affectation (avec EPISTAXIS) :
– 0 : Non – 1 : Oui |
| Randomisation group (GROUP) :
– 1 : Intravenous morphine – 2 : Intranasal Sufentanil | Groupe de randomisation (GROUP2) issue d’une affectation (avec GROUP) :
– 1 : Morphine intraveineuse – 2 : Sufentanil intranasal |
| Hallucinations is observed or declared (HALLUCINATIONS) :
– 0 : No – 1 : Yes | Des hallucinations sont observées ou déclarées (HALLUCINATIONS2) issue d’une affectation (avec HALLUCINATIONS) :
– 0 : Non – 1 : Oui |
| Hot_flushes are declared (HOT_FLUSHES) :
– 0 : No – 1 : Yes | Des bouffées de chaleur sont déclarées (HOT_FLUSHES2) issue d’une affectation (avec HOT_FLUSHES) :
– 0 : Non – 1 : Oui |
| A systolic blood pressure <90 mmHg is observed (HYPOTENSION) :
– 0 : No – 1 : Yes | Une pression artérielle systolique < 90 mmHg est observée (HYPOTENSION2) issue d’une affectation (avec HYPOTENSION) :
– 0 : Non – 1 : Oui |
| An SpO2 <90% is observed (HYPOXEMIA) :
– 0 : No – 1 : Yes | Une SpO2 < 90% est observée (HYPOXEMIA2) issue d’une affectation (avec HYPOXEMIA) :
– 0 : Non – 1 : Oui |
| Nausea is observed or declared (NAUSEA) :
– 0 : No – 1 : Yes | Des nausées sont observées ou déclarées (NAUSEA2) issue d’une affectation (avec NAUSEA) :
– 0 : Non – 1 : Oui |
| Patient required antidotal (naloxone) use (NAXOLONE) :
– 0 : No – 1 : Yes | Utilisation d’antidotes (naloxone) requise par le patient (NAXOLONE2) issue d’une affectation (avec NAXOLONE) :
– 0 : Non – 1 : Oui |
| Numerical pain rating scale at t10 (NRS_T10) | |
| Numerical pain rating scale at t20 (NRS_T20) | |
| Échelle numérique d’évaluation de la douleur à t0 (NRS_T0) | |
| Échelle numérique d’évaluation de la douleur à t30 (NRS_T30) | Échelle numérique d’évaluation de la douleur (NRS) issue d’un listage (de NRS_T0 NRS_T10 NRS_T20 NRS_T30) |
| Échelle numérique d’évaluation de la douleur à t0 (NRS_T0) | |
| Échelle numérique d’évaluation de la douleur à t30 (NRS_T30) | Difference NRS entre la première administration et à 30 minutes (NRS2) issue d’une affectation (avec NRS_T30 NRS_T0) |
| REPETITIONS | Temps (ORD_COD_TIME) issue d’une ordinalisation :
– 1 : A la ligne de base – 2 : A 10 minutes – 3 : A 20 minutes – 4 : A 30 minutes |
| REPETITIONS | |
| Randomisation group (GROUP) :
– 1 : Intravenous morphine – 2 : Intranasal Sufentanil | Temps selon Groupe de randomisation (ORD_GROUP2_COD_TIME) issue d’une ordinalisation :
– 1 : Morphine intraveineuse, A la ligne de base – 2 : Morphine intraveineuse, A 10 minutes – 3 : Morphine intraveineuse, A 20 minutes – 4 : Morphine intraveineuse, A 30 minutes – 5 : Sufentanil intranasal, A la ligne de base – 6 : Sufentanil intranasal, A 10 minutes – 7 : Sufentanil intranasal, A 20 minutes – 8 : Sufentanil intranasal, A 30 minutes |
| REPETITIONS | |
| Randomisation group (GROUP) :
– 1 : Intravenous morphine – 2 : Intranasal Sufentanil | Temps selon Groupe de randomisation (ORD_GROUP2_COD_TIME2) issue d’une ordinalisation :
– 1 : Sufentanil intranasal, A la ligne de base – 2 : Morphine intraveineuse, A la ligne de base – 3 : Sufentanil intranasal, A 10 minutes – 4 : Morphine intraveineuse, A 10 minutes – 5 : Sufentanil intranasal, A 20 minutes – 6 : Morphine intraveineuse, A 20 minutes – 7 : Sufentanil intranasal, A 30 minutes – 8 : Morphine intraveineuse, A 30 minutes |
| Sex (SEX) :
– 1 : Male – 2 : Female | Sexe (SEX2) issue d’une affectation (avec SEX) :
– 1 : Masculin – 2 : Féminin |
| Tableau 1 : Codages |
| 1. Profil d’étude |
| 1.1. Flowchart |
| [Haut de page] |
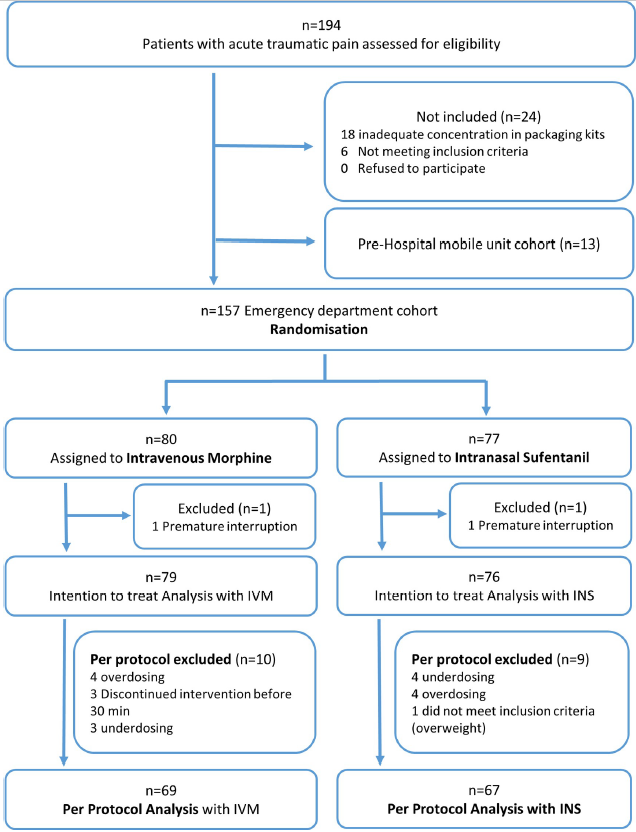
| Flowchart |
| Parmi les 194 patients inclus, 157 ont été randomisés et 136 ont respecté les administrations du protocole : 69 étaient dans le groupe IVM, 67 dans le groupe INS (population per protocole). |
| 2. Résultats dans la population per protocole |
| 2.1. Caractéristiques de base des participants |
| [Haut de page] |
| Les caractéristiques de base sont comparables entre les groupes. |
| Population | Groupe de randomisation (GROUP2) | |||||||
|---|---|---|---|---|---|---|---|---|
| _ | Morphine intraveineuse | Sufentanil intranasal | ||||||
| N=136 | N=69 | N=67 | ||||||
| Moy±SD
Méd(Q1Q3) Min-Max IC95% ou | Moy±SD
Méd(Q1Q3) Min-Max IC95% ou | Moy±SD
Méd(Q1Q3) Min-Max IC95% ou | Statistique | |||||
| Variable | n | %col | n | %col | n | %col | p | |
| Age (AGE) | Moyenne ±SD | 42,13 | ±15,92 | 41,71 | ±16,21 | 42,55 | ±15,73 | Sd p = 0,7591 |
| Médiane (Q1-Q3) | 39 | (29-54,5) | 41 | (28-54) | 38 | (30-55) | ||
| Min-Max | 18 | 75 | 18 | 72 | 19 | 75 | ||
| IC à 95% | 39,42 | 44,83 | 37,82 | 45,6 | 38,71 | 46,39 | ||
| Sexe (SEX2) | Masculin | 71 | 52,2 | 40 | 58 | 31 | 46,3 | K2 p = 0,1720 |
| Féminin | 65 | 47,8 | 29 | 42 | 36 | 53,7 | ||
| Total | 136 | 100 | 69 | 50,7 | 67 | 49,3 | ||
| Fréquence cardiaque à t0 (HR_T0) | Moyenne ±SD | 77,75 | ±14,08 | 79,57 | ±15,21 | 75,88 | ±12,66 | Sd p = 0,1275 |
| Médiane (Q1-Q3) | 75 | (67,5-87,5) | 76 | (68-91) | 74 | (67-85) | ||
| Min-Max | 48 | 119 | 53 | 119 | 48 | 108 | ||
| IC à 95% | 75,36 | 80,14 | 75,91 | 83,22 | 72,79 | 78,97 | ||
| Fréquence respiratoire à t0 (RR_T0) | Moyenne ±SD | 17,4 | ±4,31 | 16,95 | ±4,5 | 17,83 | ±4,1 | Sd p = 0,2492 |
| Médiane (Q1-Q3) | 17 | (15-20) | 16 | (15-18,5) | 18 | (15-20) | ||
| Min-Max | 10 | 40 | 10 | 40 | 11 | 32 | ||
| IC à 95% | 16,64 | 18,15 | 15,83 | 18,08 | 16,81 | 18,85 | ||
| Saturation en oxygène à t0 (SPO2_T0) | Moyenne ±SD | 98,26 | ±1,78 | 98,2 | ±1,88 | 98,31 | ±1,68 | Sd p = 0,7182 |
| Médiane (Q1-Q3) | 99 | (97-100) | 99 | (97-100) | 99 | (97-100) | ||
| Min-Max | 92 | 100 | 92 | 100 | 92 | 100 | ||
| IC à 95% | 97,96 | 98,56 | 97,75 | 98,65 | 97,9 | 98,72 | ||
| Pression artérielle diastolique à t0 (DIASTOLIC_AP_T0) | Moyenne ±SD | 79,17 | ±11,73 | 80,3 | ±11,47 | 78 | ±11,97 | Sd p = 0,2535 |
| Médiane (Q1-Q3) | 80 | (71-87) | 81 | (73-87) | 78 | (70-86) | ||
| Min-Max | 51 | 106 | 51 | 106 | 51 | 105 | ||
| IC à 95% | 77,18 | 81,16 | 77,55 | 83,06 | 75,08 | 80,92 | ||
| Échelle numérique d’évaluation de la douleur à t0 (NRS_T0) | Moyenne ±SD | 7,76 | ±1,21 | 7,61 | ±1,15 | 7,93 | ±1,25 | Sd p = 0,1264 |
| Médiane (Q1-Q3) | 8 | (7-8) | 8 | (7-8) | 8 | (7-9) | ||
| Min-Max | 6 | 10 | 6 | 10 | 6 | 10 | ||
| IC à 95% | 7,56 | 7,97 | 7,33 | 7,89 | 7,62 | 8,23 | ||
| Analgésique de secours administré après t30 (RESCUE_ANALGESIC) | Yes | 32 | 23,5 | 16 | 23,2 | 16 | 23,9 | K2 p = 0,9242 |
| No | 104 | 76,5 | 53 | 76,8 | 51 | 76,1 | ||
| Total | 136 | 100 | 69 | 50,7 | 67 | 49,3 | ||
| Centre d’inclusion (CENTRE2) | Albertville | 6 | 4,4 | 3 | 4,3 | 3 | 4,5 | |
| Annecy | 17 | 12,5 | 9 | 13 | 8 | 11,9 | ||
| Chambery | 7 | 5,1 | 4 | 5,8 | 3 | 4,5 | ||
| Grenoble (Site nord) | 83 | 61 | 41 | 59,4 | 42 | 62,7 | ||
| Grenoble (Site sud) | 4 | 2,9 | 2 | 2,9 | 2 | 3 | ||
| Saint-Jean-de-Maurienne | 18 | 13,2 | 10 | 14,5 | 8 | 11,9 | ||
| Voiron | 1 | 0,7 | 0 | 0 | 1 | 1,5 | ||
| Total | 136 | 100 | 69 | 50,7 | 67 | 49,3 | ||
| K2 : Khi2, Sd : Student | ||||||||
| Tableau 2 : Résultats dans la population per protocole – Caractéristiques de base des participants – Tri croisé |
| # Fréquence respiratoire à t0 (RR_T0) : 7 données non disponibles, 2 individus dont l’item « Groupe de randomisation (GROUP2) » est renseigné « Sufentanil intranasal » et 5 individus dont l’item « Groupe de randomisation (GROUP2) » est renseigné « Morphine intraveineuse » |
| 2.2. Résultats entre les groupes à la ligne de base et à 30 minutes |
| [Haut de page] |
| Comme décrit dans le tableau ci-dessous, l’évaluation NRS moyenne passe de 7,61 à la première administration à 3,52 à 30 minutes dans le groupe IVM et de 7,93 à 2,73 dans le groupe INS. |
| Temps selon Groupe de randomisation | |||||
|---|---|---|---|---|---|
| Morphine intraveineuse, A la ligne de base | Morphine intraveineuse, A 30 minutes | Sufentanil intranasal, A la ligne de base | Sufentanil intranasal, A 30 minutes | ||
| N=69 | N=69 | N=67 | N=67 | ||
| Variable | Moy±SD
Méd(Q1Q3) Min-Max IC95% | Moy±SD
Méd(Q1Q3) Min-Max IC95% | Moy±SD
Méd(Q1Q3) Min-Max IC95% | Moy±SD
Méd(Q1Q3) Min-Max IC95% | |
| Échelle numérique d’évaluation de la douleur (NRS) | Moyenne ±SD | 7,61±1,15 | 3,52±1,92 | 7,93±1,25 | 2,73±2,12 |
| Médiane (Q1-Q3) | 8(7-8) | 4(2-4) | 8(7-9) | 2(1-4) | |
| Min-Max | 6-10 | 0-9 | 6-10 | 0-8 | |
| IC à 95% | 7,33-7,89 | 3,06-3,98 | 7,62-8,23 | 2,21-3,25 | |
| Tableau 3 : Résultats dans la population per protocole – Résultats entre les groupes à la ligne de base et à 30 minutes – Tri croisé |
| 2.3. Analyse de la réduction NRS entre les groupes |
| [Haut de page] |
| La non-infériorité est respectée, car la valeur inférieure de l’intervalle de confiance à 97,5% de 0,286 est supérieure à la valeur de non-infériorité prédéfinie de -1,3 (différence moyenne de variation NRS entre les groupes : 1,107, IC à 97,5% 0,286 à 1,928). |
| Difference NRS entre la première administration et à 30 minutes (NRS2) | |||
|---|---|---|---|
| N=136 | |||
| Variable | MD*[IC97.5%] | ||
| Groupe de randomisation (GROUP2) | Morphine intraveineuse | 0 | n=136 |
| Sufentanil intranasal | 1,107[ 0,286 ; 1,928] | ||
| *MD : Mean Difference | |||
| Tableau 4 : Résultats dans la population per protocole – Analyse de la réduction NRS entre les groupes – Forces d’association en analyses univariées |
| 2.4. Analyse de l’évaluation NRS avec des modèles mixtes linéaires univariés |
| [Haut de page] |
| Un effet significatif du traitement est observé sur l’évaluation NRS en fonction du temps en modèle mixte linéaire univarié (p < 0,0001). |
| Échelle numérique d’évaluation de la douleur (NRS) | |||
|---|---|---|---|
| N=544 | |||
| Variable | MD*[IC95%] | p | |
| Temps (ORD_COD_TIME) | A la ligne de base | 0 | Wd p < 0,0001
n=544 |
| A 10 minutes | -2,243[-2,534 ; -1,951] | ||
| A 20 minutes | -3,772[-4,124 ; -3,420] | ||
| A 30 minutes | -4,632[-4,997 ; -4,268] | ||
| Temps selon Groupe de randomisation (ORD_GROUP2_COD_TIME) | Morphine intraveineuse, A la ligne de base | 0 | Wd p < 0,0001
n=544 |
| Morphine intraveineuse, A 10 minutes | -2,391[-2,793 ; -1,989] | ||
| Morphine intraveineuse, A 20 minutes | -3,478[-3,956 ; -3,000] | ||
| Morphine intraveineuse, A 30 minutes | -4,087[-4,552 ; -3,622] | ||
| Sufentanil intranasal, A la ligne de base | 0,317[-0,084 ; 0,718] | ||
| Sufentanil intranasal, A 10 minutes | -1,773[-2,322 ; -1,224] | ||
| Sufentanil intranasal, A 20 minutes | -3,758[-4,334 ; -3,182] | ||
| Sufentanil intranasal, A 30 minutes | -4,877[-5,449 ; -4,305] | ||
| Wd : Wald *MD : Mean Difference | |||
| Tableau 5 : Résultats dans la population per protocole – Analyse de l’évaluation NRS avec des modèles mixtes linéaires univariés – Forces d’association en analyses univariées |
| 2.5. Analyse de l’évaluation NRS avec un modèle mixte linéaire multivarié |
| [Haut de page] |
| Dans le modèle mixte linéaire multivarié :
– Une diminution significative de l’évaluation NRS est observée en fonction du temps (p < 0,0001). – Une association est observée entre le traitement et l’évaluation NRS à 30 minutes (MD -0,790, IC à 95% -1,466 à -0,114). |
| Échelle numérique d’évaluation de la douleur (NRS) | |||
|---|---|---|---|
| N=544 | n=544 | ||
| Variable | MD*[IC95%] | Wd p | |
| Groupe de randomisation (GROUP2) | Morphine intraveineuse | 0 | 0,8968 |
| Sufentanil intranasal | 0,317[-0,084 ; 0,718] | ||
| Temps (ORD_COD_TIME) | A la ligne de base | 0 | < 0,0001 |
| A 10 minutes | -2,391[-2,793 ; -1,989] | ||
| A 20 minutes | -3,478[-3,956 ; -3,000] | ||
| A 30 minutes | -4,087[-4,552 ; -3,622] | ||
| Wd : Wald *MD : Mean Difference | |||
| Tableau 6 : Résultats dans la population per protocole – Analyse de l’évaluation NRS avec un modèle mixte linéaire multivarié – Forces d’association en analyse multivariée |
| Description | MD*[IC95%] |
|---|---|
| GROUP2 Sufentanil intranasal vs Morphine intraveineuse dans ORD_COD_TIME A 10 minutes | 0,618[-0,024 ; 1,261] |
| GROUP2 Sufentanil intranasal vs Morphine intraveineuse dans ORD_COD_TIME A 20 minutes | -0,280[-0,991 ; 0,431] |
| GROUP2 Sufentanil intranasal vs Morphine intraveineuse dans ORD_COD_TIME A 30 minutes | -0,790[-1,466 ; -0,114] |
| GROUP2 Sufentanil intranasal vs Morphine intraveineuse dans ORD_COD_TIME A la ligne de base | 0,317[-0,084 ; 0,718] |
| Tableau 7 : Résultats dans la population per protocole – Analyse de l’évaluation NRS avec un modèle mixte linéaire multivarié – Description des forces d’association en analyse multivariée |
| 2.6. NRS aux différents temps d’administration par groupe |
| [Haut de page] |
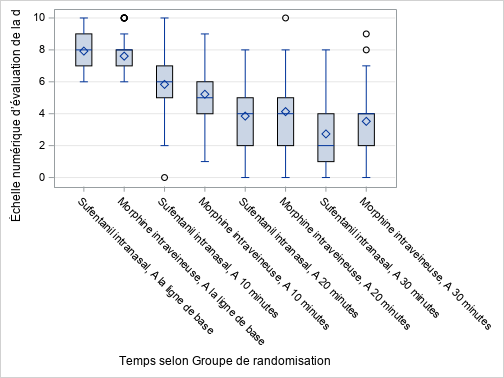 |
| Figure 2 : Résultats dans la population per protocole – NRS aux différents temps d’administration par groupe – Graphiques |
| 2.7. Effets indésirables observés |
| [Haut de page] |
| Il n’y a pas de différences statistiquement significatives entre les groupes concernant les événements indésirables légers ou graves enregistrés. |
| Groupe de randomisation | ||||||
|---|---|---|---|---|---|---|
| Morphine intraveineuse | Sufentanil intranasal | |||||
| N=69 | N=67 | Statistique | ||||
| Variable | n | %col | n | %col | p | |
| Une SpO2 < 90% est observée (HYPOXEMIA2) | Oui | 1 | 1,4 | 3 | 4,5 | Fs p = 0,3621 |
| Une pression artérielle systolique < 90 mmHg est observée (HYPOTENSION2) | Oui | 1 | 1,4 | 1 | 1,5 | Fs p = 1,0000 |
| Une fréquence respiratoire <10/minute est observée (BRADYPNEA2) | Oui | 0 | 0 | 2 | 3 | Fs p = 0,2408 |
| Un choc anaphylactique est observé (ANAPHYLACTIC_SHOCK2) | Non | 69 | 100 | 67 | 100 | |
| Un score de Ramsay > 2 est observé (COMA2) | Non | 69 | 100 | 67 | 100 | |
| Une fréquence cardiaque bpm <45/min est observée (BRADYCARDIA2) | Non | 69 | 100 | 67 | 100 | |
| Utilisation d’antidotes (naloxone) requise par le patient (NAXOLONE2) | Non | 68 | 100 | 67 | 100 | |
| Des vertiges sont observés ou déclarés (DIZZINESS2) | Oui | 25 | 36,2 | 19 | 28,4 | K2 p = 0,3265 |
| Des bouffées de chaleur sont déclarées (HOT_FLUSHES2) | Oui | 20 | 29 | 12 | 17,9 | K2 p = 0,1279 |
| Des nausées sont observées ou déclarées (NAUSEA2) | Oui | 13 | 18,8 | 8 | 11,9 | K2 p = 0,2655 |
| Le mauvais goût est déclaré (BAD_TASTE2) | Oui | 3 | 4,3 | 2 | 3 | Fs p = 1,0000 |
| Une allergie est observée (ALLERGY2) | Oui | 1 | 1,4 | 1 | 1,5 | Fs p = 1,0000 |
| L’épistaxis est observée ou déclarée (EPISTAXIS2) | Oui | 1 | 1,4 | 0 | 0 | Fs p = 1,0000 |
| Des hallucinations sont observées ou déclarées (HALLUCINATIONS2) | Non | 69 | 100 | 67 | 100 | |
| K2 : Khi2, Fs : Fisher | ||||||
| Tableau 8 : Résultats dans la population per protocole – Effets indésirables observés – Tri croisé |
| # Utilisation d’antidotes (naloxone) requise par le patient (NAXOLONE2) : 1 donnée non disponible, 1 individu dont l’item « Groupe de randomisation (GROUP2) » est renseigné « Morphine intraveineuse » |
| 3. Résultats dans la population en intention de traiter |
| 3.1. Caractéristiques de base des participants |
| [Haut de page] |
| Les caractéristiques de base sont comparables entre les groupes. |
| Population | Groupe de randomisation (GROUP2) | |||||||
|---|---|---|---|---|---|---|---|---|
| _ | Morphine intraveineuse | Sufentanil intranasal | ||||||
| N=155 | N=79 | N=76 | ||||||
| Moy±SD
Méd(Q1Q3) Min-Max IC95% ou | Moy±SD
Méd(Q1Q3) Min-Max IC95% ou | Moy±SD
Méd(Q1Q3) Min-Max IC95% ou | Statistique | |||||
| Variable | n | %col | n | %col | n | %col | p | |
| Age (AGE) | Moyenne ±SD | 42,36 | ±16,18 | 42,01 | ±16,68 | 42,72 | ±15,76 | Sd p = 0,7855 |
| Médiane (Q1-Q3) | 40 | (29-55) | 41 | (25-56) | 39,5 | (30-54,5) | ||
| Min-Max | 18 | 75 | 18 | 73 | 19 | 75 | ||
| IC à 95% | 39,79 | 44,93 | 38,28 | 45,75 | 39,12 | 46,33 | ||
| Sexe (SEX2) | Masculin | 83 | 53,5 | 47 | 59,5 | 36 | 47,4 | K2 p = 0,1303 |
| Féminin | 72 | 46,5 | 32 | 40,5 | 40 | 52,6 | ||
| Total | 155 | 100 | 79 | 51 | 76 | 49 | ||
| Fréquence cardiaque à t0 (HR_T0) | Moyenne ±SD | 77,62 | ±14 | 79,05 | ±14,96 | 76,16 | ±12,89 | Sd p = 0,2009 |
| Médiane (Q1-Q3) | 76 | (68-87) | 76 | (68-91) | 75 | (67-85) | ||
| Min-Max | 48 | 119 | 52 | 119 | 48 | 108 | ||
| IC à 95% | 75,39 | 79,85 | 75,68 | 82,42 | 73,21 | 79,1 | ||
| Fréquence respiratoire à t0 (RR_T0) | Moyenne ±SD | 17,59 | ±4,46 | 17,07 | ±4,57 | 18,09 | ±4,33 | Sd p = 0,1680 |
| Médiane (Q1-Q3) | 17 | (15-20) | 16 | (15-20) | 18 | (15-20) | ||
| Min-Max | 10 | 40 | 10 | 40 | 11 | 32 | ||
| IC à 95% | 16,86 | 18,33 | 15,99 | 18,15 | 17,09 | 19,1 | ||
| Saturation en oxygène à t0 (SPO2_T0) | Moyenne ±SD | 98,23 | ±1,79 | 98,14 | ±1,87 | 98,33 | ±1,7 | Sd p = 0,5155 |
| Médiane (Q1-Q3) | 99 | (97-100) | 99 | (97-100) | 99 | (97-100) | ||
| Min-Max | 92 | 100 | 92 | 100 | 92 | 100 | ||
| IC à 95% | 97,95 | 98,52 | 97,72 | 98,56 | 97,94 | 98,72 | ||
| Pression artérielle diastolique à t0 (DIASTOLIC_AP_T0) | Moyenne ±SD | 79,53 | ±11,64 | 80,1 | ±11,52 | 78,95 | ±11,82 | Sd p = 0,5399 |
| Médiane (Q1-Q3) | 80 | (72-87) | 80,5 | (73-87) | 80 | (70-87) | ||
| Min-Max | 51 | 106 | 51 | 106 | 51 | 105 | ||
| IC à 95% | 77,68 | 81,39 | 77,51 | 82,7 | 76,25 | 81,65 | ||
| Échelle numérique d’évaluation de la douleur à t0 (NRS_T0) | Moyenne ±SD | 7,75 | ±1,21 | 7,7 | ±1,16 | 7,82 | ±1,26 | Sd p = 0,5395 |
| Médiane (Q1-Q3) | 8 | (7-8) | 8 | (7-8) | 8 | (7-9) | ||
| Min-Max | 6 | 10 | 6 | 10 | 6 | 10 | ||
| IC à 95% | 7,56 | 7,95 | 7,44 | 7,96 | 7,53 | 8,1 | ||
| Analgésique de secours administré après t30 (RESCUE_ANALGESIC) | Yes | 37 | 23,9 | 18 | 22,8 | 19 | 25 | K2 p = 0,7464 |
| No | 118 | 76,1 | 61 | 77,2 | 57 | 75 | ||
| Total | 155 | 100 | 79 | 51 | 76 | 49 | ||
| Centre d’inclusion (CENTRE2) | Albertville | 6 | 3,9 | 3 | 3,8 | 3 | 3,9 | |
| Annecy | 19 | 12,3 | 10 | 12,7 | 9 | 11,8 | ||
| Chambery | 8 | 5,2 | 4 | 5,1 | 4 | 5,3 | ||
| Grenoble (Site nord) | 95 | 61,3 | 49 | 62 | 46 | 60,5 | ||
| Grenoble (Site sud) | 4 | 2,6 | 2 | 2,5 | 2 | 2,6 | ||
| Saint-Jean-de-Maurienne | 22 | 14,2 | 11 | 13,9 | 11 | 14,5 | ||
| Voiron | 1 | 0,6 | 0 | 0 | 1 | 1,3 | ||
| Total | 155 | 100 | 79 | 51 | 76 | 49 | ||
| K2 : Khi2, Sd : Student | ||||||||
| Tableau 9 : Résultats dans la population en intention de traiter – Caractéristiques de base des participants – Tri croisé |
| # Fréquence cardiaque à t0 (HR_T0) : 1 donnée non disponible, 1 individu dont l’item « Groupe de randomisation (GROUP2) » est renseigné « Morphine intraveineuse » |
| # Fréquence respiratoire à t0 (RR_T0) : 10 données non disponibles, 2 individus dont l’item « Groupe de randomisation (GROUP2) » est renseigné « Sufentanil intranasal » et 8 individus dont l’item « Groupe de randomisation (GROUP2) » est renseigné « Morphine intraveineuse » |
| # Saturation en oxygène à t0 (SPO2_T0) : 1 donnée non disponible, 1 individu dont l’item « Groupe de randomisation (GROUP2) » est renseigné « Morphine intraveineuse » |
| # Pression artérielle diastolique à t0 (DIASTOLIC_AP_T0) : 1 donnée non disponible, 1 individu dont l’item « Groupe de randomisation (GROUP2) » est renseigné « Morphine intraveineuse » |
| 3.2. Résultats entre les groupes à la ligne de base et à 30 minutes |
| [Haut de page] |
| Comme décrit dans le tableau ci-dessous, l’évaluation NRS moyenne passe de 7,7 à la première administration à 3,38 à 30 minutes dans le groupe IVM et de 7,82 à 2,72 dans le groupe INS. |
| Temps selon Groupe de randomisation | |||||
|---|---|---|---|---|---|
| Morphine intraveineuse, A la ligne de base | Morphine intraveineuse, A 30 minutes | Sufentanil intranasal, A la ligne de base | Sufentanil intranasal, A 30 minutes | ||
| N=79 | N=79 | N=76 | N=76 | ||
| Variable | Moy±SD
Méd(Q1Q3) Min-Max IC95% | Moy±SD
Méd(Q1Q3) Min-Max IC95% | Moy±SD
Méd(Q1Q3) Min-Max IC95% | Moy±SD
Méd(Q1Q3) Min-Max IC95% | |
| Échelle numérique d’évaluation de la douleur (NRS) | Moyenne ±SD | 7,7±1,16 | 3,38±1,93 | 7,82±1,26 | 2,72±2,18 |
| Médiane (Q1-Q3) | 8(7-8) | 3(2-4) | 8(7-9) | 2(1-4) | |
| Min-Max | 6-10 | 0-9 | 6-10 | 0-9 | |
| IC à 95% | 7,44-7,96 | 2,94-3,82 | 7,53-8,1 | 2,22-3,22 | |
| Tableau 10 : Résultats dans la population en intention de traiter – Résultats entre les groupes à la ligne de base et à 30 minutes – Tri croisé |
| # Échelle numérique d’évaluation de la douleur (NRS) : 4 données non disponibles, 1 individu dont l’item « Temps selon Groupe de randomisation (ORD_GROUP2_COD_TIME) » est renseigné « Sufentanil intranasal, A 30 minutes » et 3 individus dont l’item « Temps selon Groupe de randomisation (ORD_GROUP2_COD_TIME) » est renseigné « Morphine intraveineuse, A 30 minutes » |
| 3.3. Analyse de la réduction NRS entre les groupes |
| [Haut de page] |
| La non-infériorité est respectée, car la valeur inférieure de l’intervalle de confiance à 97,5% de 0,014 est supérieure à la valeur de non-infériorité pré-définie de -1,3 (différence moyenne de variation NRS entre les groupes : 0,817, 97,5% IC 0,014 à 1,621). |
| Difference NRS entre la première administration et à 30 minutes (NRS2) | |||
|---|---|---|---|
| N=151 | |||
| Variable | MD*[IC97.5%] | ||
| Groupe de randomisation (GROUP2) | Morphine intraveineuse | 0 | n=151 |
| Sufentanil intranasal | 0,817[ 0,014 ; 1,621] | ||
| *MD : Mean Difference | |||
| Tableau 11 : Résultats dans la population en intention de traiter – Analyse de la réduction NRS entre les groupes – Forces d’association en analyses univariées |
| 3.4. Analyse de l’évaluation NRS avec des modèles mixtes linéaires univariés |
| [Haut de page] |
| Un effet significatif du traitement est observé sur l’évaluation NRS en fonction du temps dans le modèle mixte linéaire univarié (p < 0,0001). |
| Échelle numérique d’évaluation de la douleur (NRS) | |||
|---|---|---|---|
| N=614 | |||
| Variable | MD*[IC95%] | p | |
| Temps (ORD_COD_TIME) | A la ligne de base | 0 | Wd p < 0,0001
n=614 |
| A 10 minutes | -2,381[-2,673 ; -2,088] | ||
| A 20 minutes | -3,846[-4,183 ; -3,510] | ||
| A 30 minutes | -4,702[-5,053 ; -4,351] | ||
| Temps selon Groupe de randomisation (ORD_GROUP2_COD_TIME) | Morphine intraveineuse, A la ligne de base | 0 | Wd p < 0,0001
n=614 |
| Morphine intraveineuse, A 10 minutes | -2,658[-3,083 ; -2,233] | ||
| Morphine intraveineuse, A 20 minutes | -3,683[-4,151 ; -3,215] | ||
| Morphine intraveineuse, A 30 minutes | -4,315[-4,774 ; -3,856] | ||
| Sufentanil intranasal, A la ligne de base | 0,120[-0,260 ; 0,499] | ||
| Sufentanil intranasal, A 10 minutes | -1,973[-2,490 ; -1,455] | ||
| Sufentanil intranasal, A 20 minutes | -3,894[-4,441 ; -3,346] | ||
| Sufentanil intranasal, A 30 minutes | -4,976[-5,528 ; -4,425] | ||
| Wd : Wald *MD : Mean Difference | |||
| Tableau 12 : Résultats dans la population en intention de traiter – Analyse de l’évaluation NRS avec des modèles mixtes linéaires univariés – Forces d’association en analyses univariées |
| 3.5. Analyse de l’évaluation NRS avec un modèle mixte linéaire multivarié |
| [Haut de page] |
| Dans le modèle mixte linéaire multivarié :
– Une diminution significative de l’évaluation NRS est observée en fonction du temps (p < 0,0001). – Une association est observée entre le traitement et l’évaluation NRS à 10 minutes (MD 0,686, IC à 95% 0,068 à 1,304) et à 30 minutes (MD -0,662, IC à 95% -1,313 à -0,010). |
| Échelle numérique d’évaluation de la douleur (NRS) | |||
|---|---|---|---|
| N=614 | n=614 | ||
| Variable | MD*[IC95%] | Wd p | |
| Groupe de randomisation (GROUP2) | Morphine intraveineuse | 0 | 0,9462 |
| Sufentanil intranasal | 0,120[-0,260 ; 0,499] | ||
| Temps (ORD_COD_TIME) | A la ligne de base | 0 | < 0,0001 |
| A 10 minutes | -2,658[-3,083 ; -2,233] | ||
| A 20 minutes | -3,683[-4,151 ; -3,215] | ||
| A 30 minutes | -4,315[-4,774 ; -3,856] | ||
| Wd : Wald *MD : Mean Difference | |||
| Tableau 13 : Résultats dans la population en intention de traiter – Analyse de l’évaluation NRS avec un modèle mixte linéaire multivarié – Forces d’association en analyse multivariée |
| Description | MD*[IC95%] |
|---|---|
| GROUP2 Sufentanil intranasal vs Morphine intraveineuse dans ORD_COD_TIME A 10 minutes | 0,686[ 0,068 ; 1,304] |
| GROUP2 Sufentanil intranasal vs Morphine intraveineuse dans ORD_COD_TIME A 20 minutes | -0,210[-0,885 ; 0,464] |
| GROUP2 Sufentanil intranasal vs Morphine intraveineuse dans ORD_COD_TIME A 30 minutes | -0,662[-1,313 ; -0,010] |
| GROUP2 Sufentanil intranasal vs Morphine intraveineuse dans ORD_COD_TIME A la ligne de base | 0,120[-0,260 ; 0,499] |
| Tableau 14 : Résultats dans la population en intention de traiter – Analyse de l’évaluation NRS avec un modèle mixte linéaire multivarié – Description des forces d’association en analyse multivariée |
| 3.6. Effets indésirables observés |
| [Haut de page] |
| Il n’y a pas de différences statistiquement significatives entre les groupes concernant les événements indésirables légers ou graves enregistrés. |
| Groupe de randomisation | ||||||
|---|---|---|---|---|---|---|
| Morphine intraveineuse | Sufentanil intranasal | |||||
| N=79 | N=76 | Statistique | ||||
| Variable | n | %col | n | %col | p | |
| Une SpO2 < 90% est observée (HYPOXEMIA2) | Oui | 1 | 1,3 | 4 | 5,3 | Fs p = 0,2038 |
| Une pression artérielle systolique < 90 mmHg est observée (HYPOTENSION2) | Oui | 1 | 1,3 | 2 | 2,6 | Fs p = 0,6153 |
| Une fréquence respiratoire <10/minute est observée (BRADYPNEA2) | Oui | 0 | 0 | 2 | 2,6 | Fs p = 0,2388 |
| Un choc anaphylactique est observé (ANAPHYLACTIC_SHOCK2) | Non | 79 | 100 | 76 | 100 | |
| Un score de Ramsay > 2 est observé (COMA2) | Non | 79 | 100 | 76 | 100 | |
| Une fréquence cardiaque bpm <45/min est observée (BRADYCARDIA2) | Oui | 0 | 0 | 1 | 1,3 | Fs p = 0,4903 |
| Utilisation d’antidotes (naloxone) requise par le patient (NAXOLONE2) | Non | 78 | 100 | 76 | 100 | |
| Des vertiges sont observés ou déclarés (DIZZINESS2) | Oui | 28 | 35,4 | 21 | 27,6 | K2 p = 0,2957 |
| Des bouffées de chaleur sont déclarées (HOT_FLUSHES2) | Oui | 22 | 27,8 | 14 | 18,4 | K2 p = 0,1647 |
| Des nausées sont observées ou déclarées (NAUSEA2) | Oui | 15 | 19 | 10 | 13,2 | K2 p = 0,3239 |
| Le mauvais goût est déclaré (BAD_TASTE2) | Oui | 3 | 3,8 | 2 | 2,6 | Fs p = 1,0000 |
| Une allergie est observée (ALLERGY2) | Oui | 1 | 1,3 | 1 | 1,3 | Fs p = 1,0000 |
| L’épistaxis est observée ou déclarée (EPISTAXIS2) | Oui | 1 | 1,3 | 0 | 0 | Fs p = 1,0000 |
| Des hallucinations sont observées ou déclarées (HALLUCINATIONS2) | Non | 79 | 100 | 76 | 100 | |
| K2 : Khi2, Fs : Fisher | ||||||
| Tableau 15 : Résultats dans la population en intention de traiter – Effets indésirables observés – Tri croisé |
| # Utilisation d’antidotes (naloxone) requise par le patient (NAXOLONE2) : 1 donnée non disponible, 1 individu dont l’item « Groupe de randomisation (GROUP2) » est renseigné « Morphine intraveineuse » |
| Tables et figures |
| Tableau 1 : Codages |
| Tableau 2 : Résultats dans la population per protocole – Caractéristiques de base des participants – Tri croisé |
| Tableau 3 : Résultats dans la population per protocole – Résultats entre les groupes à la ligne de base et à 30 minutes – Tri croisé |
| Tableau 4 : Résultats dans la population per protocole – Analyse de la réduction NRS entre les groupes – Forces d’association en analyses univariées |
| Tableau 5 : Résultats dans la population per protocole – Analyse de l’évaluation NRS avec des modèles mixtes linéaires univariés – Forces d’association en analyses univariées |
| Tableau 6 : Résultats dans la population per protocole – Analyse de l’évaluation NRS avec un modèle mixte linéaire multivarié – Forces d’association en analyse multivariée |
| Tableau 7 : Résultats dans la population per protocole – Analyse de l’évaluation NRS avec un modèle mixte linéaire multivarié – Description des forces d’association en analyse multivariée |
| Tableau 8 : Résultats dans la population per protocole – Effets indésirables observés – Tri croisé |
| Tableau 9 : Résultats dans la population en intention de traiter – Caractéristiques de base des participants – Tri croisé |
| Tableau 10 : Résultats dans la population en intention de traiter – Résultats entre les groupes à la ligne de base et à 30 minutes – Tri croisé |
| Tableau 11 : Résultats dans la population en intention de traiter – Analyse de la réduction NRS entre les groupes – Forces d’association en analyses univariées |
| Tableau 12 : Résultats dans la population en intention de traiter – Analyse de l’évaluation NRS avec des modèles mixtes linéaires univariés – Forces d’association en analyses univariées |
| Tableau 13 : Résultats dans la population en intention de traiter – Analyse de l’évaluation NRS avec un modèle mixte linéaire multivarié – Forces d’association en analyse multivariée |
| Tableau 14 : Résultats dans la population en intention de traiter – Analyse de l’évaluation NRS avec un modèle mixte linéaire multivarié – Description des forces d’association en analyse multivariée |
| Tableau 15 : Résultats dans la population en intention de traiter – Effets indésirables observés – Tri croisé |
| Figure 1 : Profil d’étude – Flowchart – Flowchart |
| Figure 2 : Résultats dans la population per protocole – NRS aux différents temps d’administration par groupe – Graphiques |
| Date de réalisation : 16 juin 2021 |
| Réalisateur : RUS |
| Logiciel version 0.1 |