| [2009-016442-74] Essai de phase II randomisé contrôlé par placebo concernant les cellules souches mésenchymateuses (MSCs) autologues dans la sclérose en plaques.
Llufriu S, Sepulveda M, Blanco Y, Marin P, Moreno B, et al. Source : PLOS ONE | https://doi.org/10.1371/journal.pone.0113936 Télécharger “Table 2009-016442-74-msc” 2009-016442-74-msc.zip – Téléchargé 4 fois – 1,24 Mo Droit d’auteur : Utilisation des données du rapport sans restriction pourvu que l’auteur original et la source soient cités (données brutes libres de droits). |
| Méthodes |
| Objectif :
Cette étude de phase II randomisée, en double aveugle, contrôlée avec placebo et appariée, étudie la sécurité et l’efficacité des cellules souches mésenchymateusee autologues chez les patients atteints de scléroses en plaques récurrente-rémittente. Evaluation : L’étude a été réalisée dans un hôpital clinique de Barcelone, Espagne, entre Novembre 2010 et Juin 2012. Neuf patients ne répondant pas au traitement conventionnel, définis par au moins 1 rechute et / ou GEL à l’IRM au cours des 12 derniers mois, d’une durée de maladie de 2 à 10 ans et d’une mesure du statut d’invalidité (EDSS) de 3,0 à 6,5, ont été randomisés pour recevoir IV 1-2E+6 bone-marrow-derives-MSCs/kg ou un Placebo. Après 6 mois, le traitement a été inversé et les patients ont été suivis pendant 6 mois supplémentaires. Le critère de jugement principal de cette étude est le changement du nombre de lésions rehaussant le gadolinium (GEL) sur le champ magnétique à l2 mois. Les critères de jugement secondaires sont (i) de nouvelles lésions ou des lésions agrandies sur des images à long temps de répétition enregistrées en série, (ii) le changement de volume cérébral et (iii) les résultats cliniques (rechutes et incapacités par EDSS et MS Functional Composite). |
| Codages et variables générées suite au gel de la base de données | |
|---|---|
| Variable(s) d’origine | Variable créée |
| Durée de la maladie (DIFONSET_ENTRY) | |
| Totalrelapses (TOTALRELAPSES) | Taux de rechute annualisé (ANNUALRELAPSES) issue d’une affectation (avec DIFONSET_ENTRY TOTALRELAPSES) |
| EDSS_12m (EDSS_12M) | |
| EDSS_6m (EDSS_6M) | |
| EDSSbasal (EDSSBASAL) | Evolution EDSS (EDSS) issue d’un listage (de EDSS_6M2 EDSS_12M2) |
| Flair_vol_12m (FLAIR_VOL_12M) | |
| Flair_vol_6m (FLAIR_VOL_6M) | |
| Flair_vol_bas (FLAIR_VOL_BAS) | Evolution du volume de lésion T2, ml (FLAIR_VOL) issue d’un listage (de FLAIR_VOL_6M2 FLAIR_VOL_12M2) |
| Flair_vol_bas (FLAIR_VOL_BAS) | Volume de lésion T2, ml (FLAIR_VOL_BAS2) issue d’une affectation (avec FLAIR_VOL_BAS) |
| Nombre de GEL (GAD_LESIONS_BASAL) | |
| Nombre de GEL cumulé (GAD_LESIONS_6M) | |
| Nombre de GEL cumulé (GAD_LESIONS_E) | Evolution du nombre de GEL (GAD_LESIONS2) issue d’un listage (de GAD_LESIONS_6M2 GAD_LESIONS_E2) |
| N_T2_new_3m (N_T2_NEW_3M) | |
| N_T2_new_6m (N_T2_NEW_6M) | |
| N_T2_new_9m (N_T2_NEW_9M) | |
| N_T2_new_D (N_T2_NEW_D) | Nombre de lésions T2 nouvelles ou agrandies (N_T2_NEW2) issue d’un listage (de N_T2_NEW_6M2 N_T2_NEW_D2) |
| Traitement de fond approuvé antérieurement (FIRSTLINE) :
– Betaferon – Ciclofosfamida – Copaxone – Rebif44 | Traitement de fond approuvé antérieurement (RECOD_FIRSTLINE) issue d’un recodage :
– 1 : Betaferon ou ciclofosfamida – 2 : Copaxone – 3 : Rebif44 |
| GENDER :
– 1 : Male – 2 : Female | Sexe (SEXE) issue d’une affectation (avec GENDER) :
– 1 : Maculin – 2 : Féminin |
| Nombre de rechutes (TOTALRELAP_1STINF) | |
| Nombre de rechutes (TOTALRELAP_2NDINF) | Nombre de rechutes (TOTALRELAP) issue d’un listage (de TOTALRELAP_1STINF TOTALRELAP_2NDINF) |
| Grupo_tto (GRUPO_TTO) | |
| REPETITIONS | Groupe (TRAIT1) issue d’un conditionnement (sur GRUPO_TTO REPETITIONS) :
– MSCs – Placebo |
| Evolution du volume cérébral, % (VOL_6MTO12M) | |
| Evolution du volume cérébral, % (VOL_BASELTO6M) | Evolution du volume cérébral, % (VOL_BASELTO) issue d’un listage (de VOL_BASELTO6M VOL_6MTO12M) |
| MSFC, z score (ZMSFCS_BASAL) | |
| ZMSFC_12m (ZMSFC_12M) | |
| ZMSFC_6m (ZMSFC_6M) | Evolution z-score MSFC (ZMSFC) issue d’un listage (de ZMSFC_6M2 ZMSFC_12M2) |
| Tableau 1 : Codages |
| Principes de l’étude | |
|---|---|
| Descriptifs | Les variables qualitatives sont décrites par leurs fréquences et leurs pourcentages par niveau.
Les variables quantitatives sont décrites par leurs moyennes et leurs écart-types, leurs quartiles, leurs minimum/maximum. |
| Associations | L’association entre un paramètre quantitatif et l’item « Groupe (TRAIT1) » a été évaluée avec le test (échantillons appariés) de Student(Sd), le test du signe de Wilcoxon(Wc) ou le test de Friedman(Fm) selon les conditions de validités.
L’association entre un paramètre qualitatif et l’item « Groupe (TRAIT1) » a été évaluée avec un test de Mc Nemar(MN) ou le test de Cochran(Cc). |
| Analyse appariée | La force d’association du traitement avec l’item « Evolution du nombre de GEL (GAD_LESIONS2) » a été évaluée et retranscrite sous forme de différences moyennes avec leurs intervalles de confiance à 95% et à l’aide de la statistique de Wald. |
| Tableau 2 : Principes d’étude |
| Flowchart |
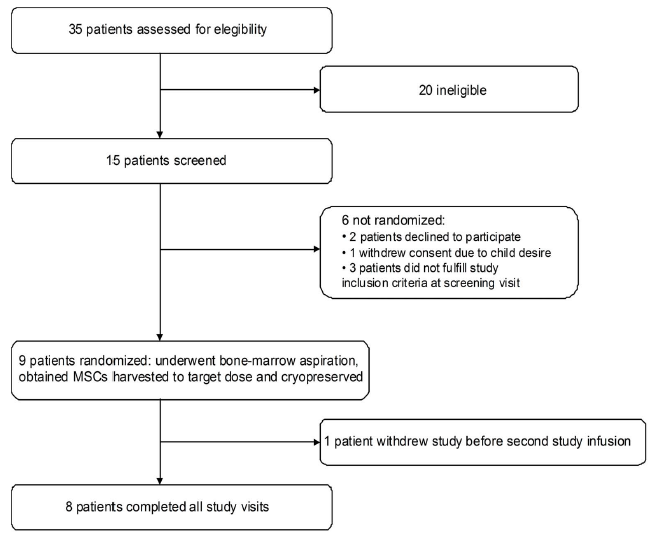 |
| Figure 1 : Flowchart |
| Résultats : Caractéristiques initiales |
| Population | Groupe (TRAIT1) | ||||||
|---|---|---|---|---|---|---|---|
| _ | MSCs | Placebo | |||||
| N=18 | N=9 | N=9 | |||||
| Moy±SD
Méd(Q1Q3) Min-Max ou | Moy±SD
Méd(Q1Q3) Min-Max ou | Moy±SD
Méd(Q1Q3) Min-Max ou | |||||
| Variable | n | %col | n | %col | n | %col | |
| Age (AGE_ENTRY) | Moyenne ±SD | 36,78 | ±8,17 | 36,78 | ±8,42 | 36,78 | ±8,42 |
| Médiane (Q1-Q3) | 41 | (30-43) | 41 | (30-43) | 41 | (30-43) | |
| Min-Max | 23 | 48 | 23 | 48 | 23 | 48 | |
| Durée de la maladie (DIFONSET_ENTRY) | Moyenne ±SD | 8,26 | ±2,52 | 8,26 | ±2,59 | 8,26 | ±2,59 |
| Médiane (Q1-Q3) | 9,08 | (7,25-9,33) | 9,08 | (7,25-9,33) | 9,08 | (7,25-9,33) | |
| Min-Max | 4,25 | 12,5 | 4,25 | 12,5 | 4,25 | 12,5 | |
| Rechutes au cours des 2 dernières années (RELAPSES_2LASTY) | Moyenne ±SD | 2,44 | ±1,29 | 2,44 | ±1,33 | 2,44 | ±1,33 |
| Médiane (Q1-Q3) | 2 | (2-3) | 2 | (2-3) | 2 | (2-3) | |
| Min-Max | 1 | 5 | 1 | 5 | 1 | 5 | |
| Rechutes au cours de la dernière année (RELAPSE_LASTYEAR) | Moyenne ±SD | 1,67 | ±0,84 | 1,67 | ±0,87 | 1,67 | ±0,87 |
| Médiane (Q1-Q3) | 1 | (1-2) | 1 | (1-2) | 1 | (1-2) | |
| Min-Max | 1 | 3 | 1 | 3 | 1 | 3 | |
| Taux de rechute annualisé (ANNUALRELAPSES) | Moyenne ±SD | 1,04 | ±0,49 | 1,04 | ±0,51 | 1,04 | ±0,51 |
| Médiane (Q1-Q3) | 0,9 | (0,63-1,52) | 0,9 | (0,63-1,52) | 0,9 | (0,63-1,52) | |
| Min-Max | 0,55 | 1,84 | 0,55 | 1,84 | 0,55 | 1,84 | |
| EDSS (EDSSATENTRY) | Moyenne ±SD | 4 | ±0,91 | 4 | ±0,94 | 4 | ±0,94 |
| Médiane (Q1-Q3) | 3,5 | (3,5-4) | 3,5 | (3,5-4) | 3,5 | (3,5-4) | |
| Min-Max | 3 | 6 | 3 | 6 | 3 | 6 | |
| Temps pour EDSS 3.0 (années) (YEDSS3) | Moyenne ±SD | 6,67 | ±1,99 | 6,67 | ±2,05 | 6,67 | ±2,05 |
| Médiane (Q1-Q3) | 7 | (5,5-7,5) | 7 | (5,5-7,5) | 7 | (5,5-7,5) | |
| Min-Max | 3,8 | 10 | 3,8 | 10 | 3,8 | 10 | |
| Temps pour EDSS 4.0 (années) (YEDSS4) | Moyenne ±SD | 7,27 | ±3,22 | 7,27 | ±3,48 | 7,27 | ±3,48 |
| Médiane (Q1-Q3) | 6,67 | (4,88-9,67) | 6,67 | (4,88-9,67) | 6,67 | (4,88-9,67) | |
| Min-Max | 3,75 | 12 | 3,75 | 12 | 3,75 | 12 | |
| Temps pour EDSS 6.0 (années) (YEDSS6) | Moyenne ±SD | 8 | ±0 | 8 | ±0 | 8 | ±0 |
| Médiane (Q1-Q3) | 8 | (8-8) | 8 | (8-8) | 8 | (8-8) | |
| Min-Max | 8 | 8 | 8 | 8 | 8 | 8 | |
| MSFC, z score (ZMSFCS_BASAL) | Moyenne ±SD | -0,3 | ±0,51 | -0,3 | ±0,52 | -0,3 | ±0,52 |
| Médiane (Q1-Q3) | -0,28 | (-0,76–0,09) | -0,28 | (-0,76–0,09) | -0,28 | (-0,76–0,09) | |
| Min-Max | -1,01 | 0,48 | -1,01 | 0,48 | -1,01 | 0,48 | |
| MSSS (MSSSENTRY) | Moyenne ±SD | 5,82 | ±1,24 | 5,82 | ±1,28 | 5,82 | ±1,28 |
| Médiane (Q1-Q3) | 5,36 | (4,93-6,78) | 5,36 | (4,93-6,78) | 5,36 | (4,93-6,78) | |
| Min-Max | 4,17 | 7,65 | 4,17 | 7,65 | 4,17 | 7,65 | |
| Nombre de GEL (GAD_LESIONS_BASAL) | Moyenne ±SD | 4,67 | ±8,07 | 4,67 | ±8,32 | 4,67 | ±8,32 |
| Médiane (Q1-Q3) | 0 | (0-3) | 0 | (0-3) | 0 | (0-3) | |
| Min-Max | 0 | 22 | 0 | 22 | 0 | 22 | |
| Volume de lésion T2, ml (FLAIR_VOL_BAS2) | Moyenne ±SD | 19,24 | ±15,74 | 19,24 | ±16,23 | 19,24 | ±16,23 |
| Médiane (Q1-Q3) | 16,27 | (12,84-20,83) | 16,27 | (12,84-20,83) | 16,27 | (12,84-20,83) | |
| Min-Max | 3,08 | 58,17 | 3,08 | 58,17 | 3,08 | 58,17 | |
| Traitement de fond approuvé antérieurement (RECOD_FIRSTLINE) | Betaferon ou ciclofosfamida | 8 | 44,4 | 4 | 44,4 | 4 | 44,4 |
| Copaxone | 4 | 22,2 | 2 | 22,2 | 2 | 22,2 | |
| Rebif44 | 6 | 33,3 | 3 | 33,3 | 3 | 33,3 | |
| Total | 18 | 100 | 9 | 50 | 9 | 50 | |
| Tableau 3 : Tri croisé des caractéristiques initiales |
| Résultats : Critère de jugement principal |
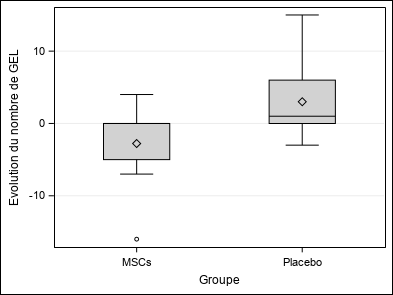
| A la fin de l’étude, aucune association n’est mise en évidence entre le groupe et le nombre de GEL (p = 0,0938 / p = 0,0612), le nombre de lésions T2 nouvelles ou agrandies (p = 0,5625), l’évolution du volume cérébral (p = 0,2031 / p = 0,2500) et les critères cliniques (p = 1,0000 / p = 0,8125 / p = 0,9453).
Cependant, une tendance à la réduction du nombre de GEL moyen par patient traité par MSCs est observée. |
| Population | Groupe (TRAIT1) | ||||
|---|---|---|---|---|---|
| _ | MSCs | Placebo | |||
| N=18 | N=9 | N=9 | Statistique | ||
| Variable | Moy±SD
Méd(Q1Q3) Min-Max | Moy±SD
Méd(Q1Q3) Min-Max | Moy±SD
Méd(Q1Q3) Min-Max | p | |
| Evolution du nombre de GEL (GAD_LESIONS2) | Moyenne ±SD | 0,11±6,22 | -2,78±5,89 | 3±5,36 | Wc p = 0,0938 |
| Médiane (Q1-Q3) | 0(-1-2) | 0(-5-0) | 1(0-6) | ||
| Min-Max | -16-15 | -16-4 | -3-15 | ||
| Wc : Wilcoxon | |||||
| Tableau 4 : Tri croisé du critère de jugement principal |
| Evolution du nombre de GEL (GAD_LESIONS2) | |||
|---|---|---|---|
| N=18 | n=18 | ||
| Variable | MD*[IC95%] | Wd p | |
| Groupe (TRAIT1) | MSCs | 0 | 0,0612 |
| Placebo | 5,778[-0,345 ; 11,900] | ||
| Wd : Wald *MD : Mean Difference | |||
| Tableau 5 : Force d’association du traitement avec le critère de jugement principal |
| Résultats : Critères de jugement secondaires |
| Population | Groupe (TRAIT1) | ||||
|---|---|---|---|---|---|
| _ | MSCs | Placebo | |||
| N=18 | N=9 | N=9 | Statistique | ||
| Variable | Moy±SD
Méd(Q1Q3) Min-Max | Moy±SD
Méd(Q1Q3) Min-Max | Moy±SD
Méd(Q1Q3) Min-Max | p | |
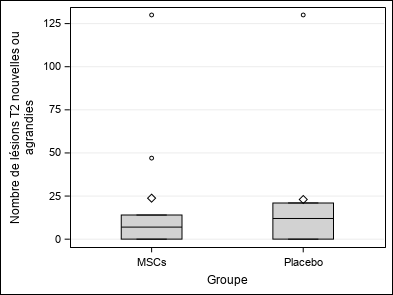
| Nombre de lésions T2 nouvelles ou agrandies (N_T2_NEW2) | Moyenne ±SD | 23,39±40,47 | 23,78±42,42 | 23±40,99 | Wc p = 0,5625 |
| Médiane (Q1-Q3) | 9(0-21) | 7(0-14) | 12(0-21) | ||
| Min-Max | 0-130 | 0-130 | 0-130 | ||
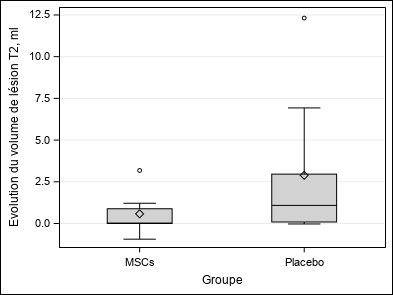
| Evolution du volume de lésion T2, ml (FLAIR_VOL) | Moyenne ±SD | 1,73±3,2 | 0,58±1,17 | 2,89±4,16 | Wc p = 0,2031 |
| Médiane (Q1-Q3) | 0,78(0-1,88) | 0,02(0-0,88) | 1,08(0,09-2,96) | ||
| Min-Max | -0,94-12,32 | -0,94-3,18 | -0,03-12,32 | ||
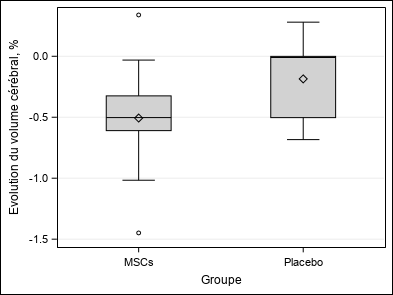
| Evolution du volume cérébral, % (VOL_BASELTO) | Moyenne ±SD | -0,35±0,46 | -0,51±0,52 | -0,19±0,34 | Wc p = 0,2500 |
| Médiane (Q1-Q3) | -0,37(-0,59-0) | -0,5(-0,61–0,32) | -0,01(-0,5-0) | ||
| Min-Max | -1,45-0,34 | -1,45-0,34 | -0,68-0,28 | ||
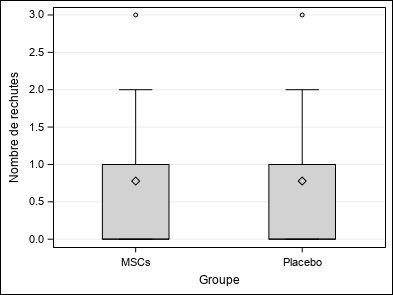
| Nombre de rechutes (TOTALRELAP) | Moyenne ±SD | 0,78±1,06 | 0,78±1,09 | 0,78±1,09 | Wc p = 1,0000 |
| Médiane (Q1-Q3) | 0(0-1) | 0(0-1) | 0(0-1) | ||
| Min-Max | 0-3 | 0-3 | 0-3 | ||
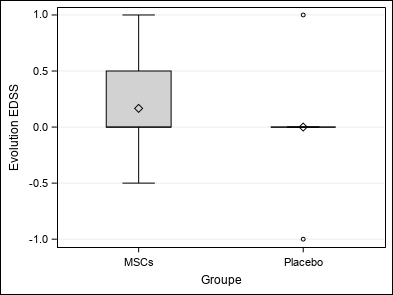
| Evolution EDSS (EDSS) | Moyenne ±SD | 0,08±0,52 | 0,17±0,56 | 0±0,5 | Wc p = 0,8125 |
| Médiane (Q1-Q3) | 0(0-0) | 0(0-0,5) | 0(0-0) | ||
| Min-Max | -1-1 | -0,5-1 | -1-1 | ||
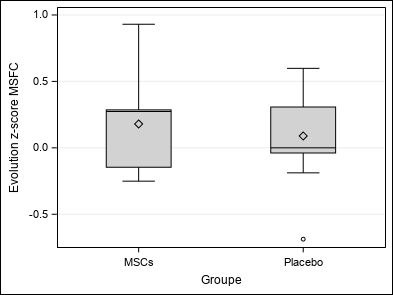
| Evolution z-score MSFC (ZMSFC) | Moyenne ±SD | 0,13±0,38 | 0,18±0,38 | 0,09±0,4 | Wc p = 0,9453 |
| Médiane (Q1-Q3) | 0,11(-0,15-0,31) | 0,27(-0,15-0,29) | 0(-0,04-0,31) | ||
| Min-Max | -0,69-0,93 | -0,25-0,93 | -0,69-0,6 | ||
| Wc : Wilcoxon | |||||
| Tableau 6 : Tri croisé des critères de jugement secondaires |
| Tables et figures |
| Tableau 1 : Codages |
| Tableau 2 : Principes d’étude |
| Tableau 3 : Tri croisé des caractéristiques initiales |
| Tableau 4 : Tri croisé du critère de jugement principal |
| Tableau 5 : Force d’association du traitement avec le critère de jugement principal |
| Tableau 6 : Tri croisé des critères de jugement secondaires |
| Figure 1 : Flowchart |
| Figure 2 : Critère de jugement principal |
| Figure 3 : Critères de jugement secondaires |
| Date de réalisation : 2 mai 2020 |
| Réalisateur : RUS |
| Logiciel version 0.1 |